ボルタ電池
ボルタ電池とは
使い捨ての電池を一次電池、充電すれば何回でも使える電池を二次電池という。
ボルタ電池とは、アレッサンドロ・ボルタ(イタリアの物理学者)が考案した一次電池である。
陽極に銅板、負極に亜鉛板、電解液に硫酸を用いた電池である。
1.1ボルト程度の起電力を持つ。
ボルタ電池の原理
まず、亜鉛板を希硫酸に入れたときの反応を確認しておこう。
亜鉛板を希硫酸に入れると、亜鉛板は溶けながら水素ガスを発生させる。
この現象は次のステップで成り立っている。
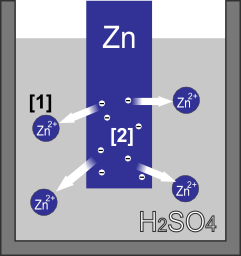
[1]亜鉛板中の亜鉛原子(Zn)が亜鉛イオン(Zn2+)となって液中へ溶け出す
[2]亜鉛イオン(Zn2+)が残した電子の影響で亜鉛板が負電荷を帯びる
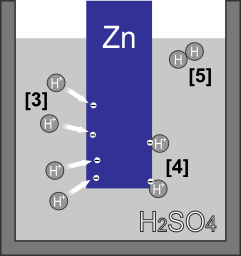
[3]陽電荷を帯びた溶液中の水素イオン(H+)が負電荷を帯びた亜鉛板に引き寄せらせる
[4]水素イオン(H+)が亜鉛板中の電子を得て水素原子(H)になる
[5]水素原子(H)どうしが結合して水素分子に(H2)になり、水素ガスとして発生する
上記のステップ[2]で残された電子を取り出せれば電池になる。
これがボルタの電池の原理なのだ。
ボルタ電池の仕組み
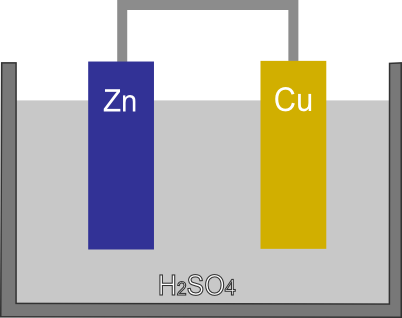
銅板は希硫酸に入れても溶けることはない。
そこで、導線で結んだ亜鉛板と銅板を同時に希硫酸に入れることにする。
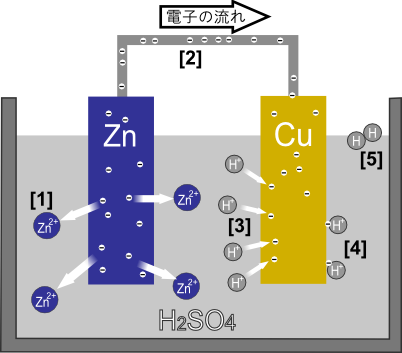
[1]亜鉛板中の亜鉛原子(Zn)が亜鉛イオン(Zn2+)となって液中へ溶け出す
[2]亜鉛イオン(Zn2+)が残した電子が銅板へと移動する
[3]陽電荷を帯びた溶液中の水素イオン(H+)が負電荷を帯びた銅板に引き寄せらせる
[4]水素イオン(H+)が銅板中の電子を得て水素原子(H)になる
[5]水素原子(H)どうしが結合して水素分子に(H2)になり、水素ガスとして発生する
負極(亜鉛板)では、亜鉛をイオン化することによって電子を取り出す。
陽極(銅板)では流れてきた電子を、水素イオン(H+)に吸収させる。
これが、ボルタの電池の原理である。
ボルタの電池の寿命は長くない。
すぐに起電力が落ちてしまう。
この現象を分極という。
次のページでボルタ電池の分極を解説する。
■次のページ:ボルタ電池の分極
スポンサーリンク
2010/03/29
2011/08/11